新的 3D 共培养模型用于研究质子治疗对侵袭性脑癌的影响
代尔夫特理工大学的研究人员受大脑微血管几何结构的启发,设计了新型 3D 工程支架。这些微结构与胶质母细胞瘤(一种侵袭性脑癌)和内皮细胞(血管的组成部分)共培养。该模型使研究人员能够研究质子治疗对胶质母细胞瘤的影响,并揭示内皮细胞对癌细胞可能的保护作用。
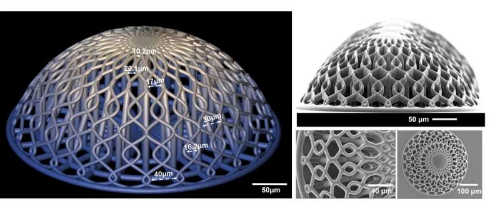
“肿瘤主要是在 2D 环境(例如培养皿)或通过动物实验进行研究。由于这些模型相距数英里,因此很难将 2D 模型的研究结果转化为人类环境,”精密与微系统工程系。“此外,使用实验动物还存在明显的伦理问题。”
Accardo 旨在弥合体外(细胞)和体内(活体)模型的差距。与他的博士学位一起。Accardo 的学生 Qais Akolawala 与荷兰质子治疗中心 (HollandPTC) 和 LUMC 的合作者开发了类似于我们大脑微血管结构的 3D 工程支架,有助于更好地了解质子治疗如何影响胶质母细胞瘤。
最大限度地减少附带损害
研究表明,细胞的行为和反应取决于外部环境,特别是环境的形状。“为了创建一个生物学相关的模型,我们需要我们的 3D 工程支架尽可能地模仿自然环境。由于胶质母细胞瘤在大脑血管周围聚集和增殖,我们在模型中设计了微小的血管和曲率,”Akolawala 解释道。
研究人员利用称为双光子聚合的微制造技术制造了这些工程微环境。首先,研究小组在制造的微结构上培养血管内皮细胞,然后培养人类恶性胶质母细胞瘤细胞。
胶质母细胞瘤是一种侵袭性非常强的癌症,预后较差。虽然手术、化疗和 X 射线放射治疗仍然是当前的标准,但质子束治疗是一种有吸引力的替代方案,因为质子可以损伤癌细胞,同时不伤害周围的健康组织。阿卡多说:“这是因为质子能够在患者体内的特定点释放能量,从而导致细胞损伤。”
由于与 X 射线相比,质子疗法是一种相对较新的技术,因此需要更好地了解质子与细胞在生理相关微环境中的相互作用,以及它对癌细胞的实际损害程度。
免责声明:本答案或内容为用户上传,不代表本网观点。其原创性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容、文字的真实性、完整性、及时性本站不作任何保证或承诺,请读者仅作参考,并请自行核实相关内容。 如遇侵权请及时联系本站删除。
